NEWS
新聞資訊
科研合作
2022年,全球癌癥死亡病例估計為970萬(wàn)(包含非黑色素瘤皮膚癌)。其中,肺癌也是導致癌癥死亡的主要原因,預計有180萬(wàn)死亡病例,占所有癌癥死亡的18.7%。流行病學(xué)數據顯示,約 10% 的非小細胞肺癌(NSCLC)患者在初診時(shí)即存在腦轉移,而 26-53% 的患者在病程中進(jìn)展為腦轉移。大樣本多瘤種長(cháng)期隊列隨訪(fǎng)發(fā)現,肺癌的腦轉移遠高于其他常見(jiàn)惡性腫瘤。攜帶表皮生長(cháng)因子受體(EGFR)突變、間變性淋巴瘤激酶(ALK)重排等驅動(dòng)基因陽(yáng)性的 NSCLC 患者,相比驅動(dòng)基因陰性患者,表現出更高的腦轉移風(fēng)險和更早的發(fā)病時(shí)間。腦轉移發(fā)生后,NSCLC 患者的總生存期顯著(zhù)降低,經(jīng)治后中位生存期(OS)僅 7-12 個(gè)月。傳統治療如放射治療和外科手術(shù)的臨床獲益有限,且常伴隨認知功能障礙和生活質(zhì)量下降。由于腦轉移細胞存在于具有生理特殊性的保護性腦屏障內,因此需要采取不同的治療策略[1]。

血腦屏障和血腫瘤屏障的示意圖[1]
近年來(lái),針對 EGFR、ALK 等靶點(diǎn)的新型小分子酪氨酸激酶抑制劑不斷涌現,有效穿透血腦屏障的同時(shí)提升了顱內藥物濃度、改善患者預后,從而打破了 NSCLC 腦轉移既往的治療格局。中國醫藥教育協(xié)會(huì )肺癌醫學(xué)教育專(zhuān)業(yè)委員會(huì )和北京醫學(xué)獎勵基金會(huì )肺癌醫學(xué)青年專(zhuān)家委員會(huì )腦轉移協(xié)作組共同制定了中國驅動(dòng)基因陽(yáng)性非小細胞肺癌腦轉移臨床診療指南[2]。該指南結合最新研究和臨床經(jīng)驗,依據多學(xué)科診療原則,包括診斷、治療時(shí)機及系統和局部治療選擇等。指南還提出了針對不同驅動(dòng)基因類(lèi)型的個(gè)體化治療策略,目的是為臨床醫師提供指導,提高中國NSCLC腦轉移的診療水平。

驅動(dòng)基因陽(yáng)性NSCLC腦轉移一般治療流程
General treatment flow for brain metastases in driver gene positive NSCLC
EGFR
● 對于EGFR 經(jīng)典突變的 NSCLC 腦轉移初始靶向治療,建議優(yōu)先考慮以下方案:奧希替尼 ± 化療(1B)[3],伏美替尼(1B)[4],貝福替尼(1B)[5],阿美替尼(1B)[6],佐利替尼(1A)[7],埃克替尼(2A)[8];也可考慮選擇埃萬(wàn)妥單抗聯(lián)合拉澤替尼方案(2B)[9]。
在主流的第三代EGFR-TKIs的臨床III期研究中,腦轉移亞組的循證醫學(xué)證據得到了充分支持。與第一代EGFR-TKIs相比,第三代EGFR-TKIs展現了更高的顱內客觀(guān)緩解率(ORR)以及延長(cháng)無(wú)進(jìn)展生存期(PFS)的效果(詳細數據請參見(jiàn)表1)。在針對EGFR陽(yáng)性腦轉移的靶向治療中,除了考慮TKIs的代際差異外,藥物穿透血腦屏障(BBB)的能力也應成為決定腦轉移靶向治療策略的關(guān)鍵因素之一。例如,奧希替尼能夠有效穿透BBB,其效果優(yōu)于第一代和第二代TKIs[10];而佐利替尼由于不受BBB上P-糖蛋白外排作用的影響,其顱內濃度顯著(zhù)提高[11]。此外,起始使用更高劑量的TKIs可能也會(huì )增加顱內濃度,從而提升治療效果。
表1 不同EGFR-TKIs在EGFR陽(yáng)性NSCLC腦轉移人群中的循證
Table1 Evidence for different EGFR-TKIs in EGFR positive NSCLC with brain metastases
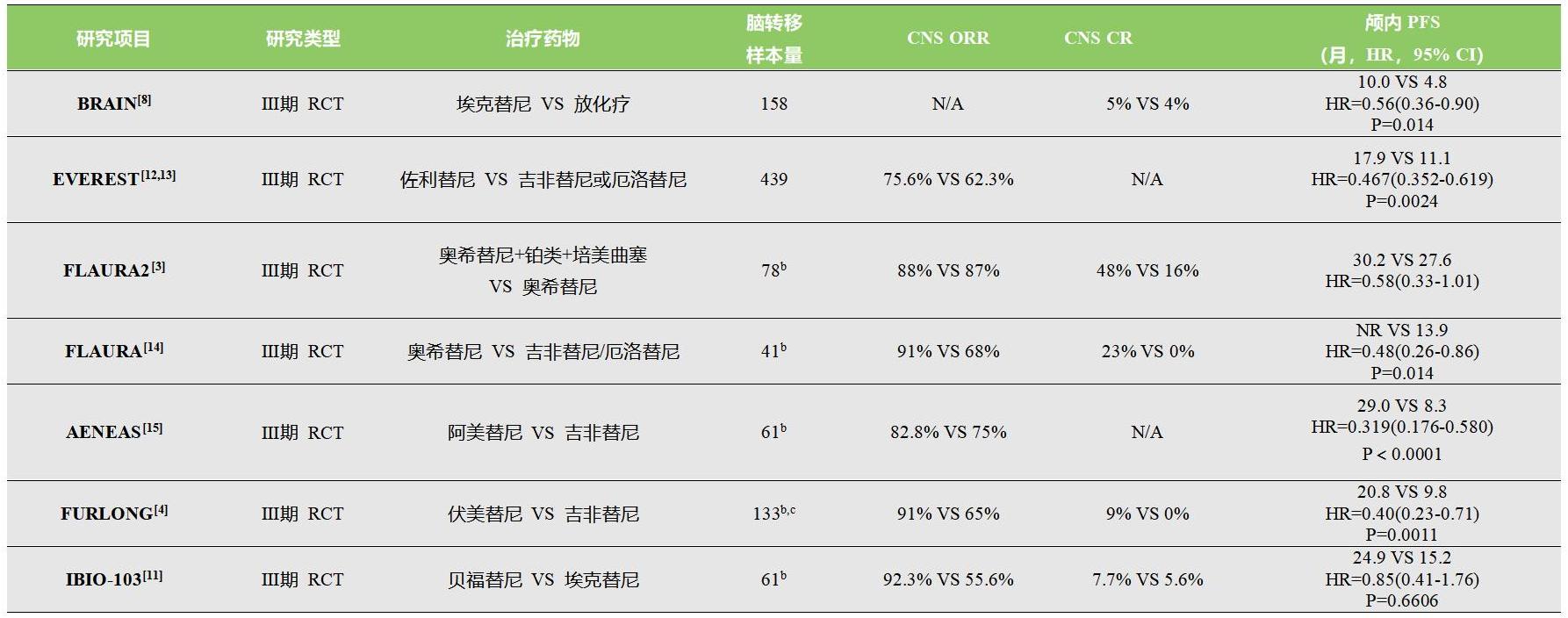
a:如無(wú)特殊標注這里專(zhuān)指cEFR人群,cEFR指的是中樞神經(jīng)系統可評估反應集。這一分析組專(zhuān)門(mén)包含那些在基線(xiàn)腦部掃描中至少有一個(gè)可測量的CNS病變的患者。與cFAS(中樞神經(jīng)系統全面分析組)不同,cEFR僅包括那些具有可測量目標CNS病變的患者。評價(jià)奧希替尼與奧希替尼+化療的療效,使用cEFR數據集確實(shí)是更好的選擇。這是因為cEFR專(zhuān)注于那些具有可測量CNS病變的患者,可以更準確地評估治療對這些特定病變的反應,從而提供更具針對性的療效數據;
b:指腦轉移亞組;
c:包含不可測量的腦轉移病變患者;
d:采用RANO-BM標準。
EGFR-TKIs:表皮生長(cháng)因子受體-酪氨酸激酶抑制劑;CNS:中樞神經(jīng)系統;ORR:客觀(guān)緩解率;CR:完全緩解;PFS:無(wú)進(jìn)展生存期;NR:未達到;HR:危險比。
● 對于已使用第一、二代 EGFR-TKIs 的 EGFR 經(jīng)典突變的 NSCLC 腦轉移患者出現 T790M 突變,推薦更換為顱內活性較高的第三代 TKIs 藥物(1B)[16]。
根據APPLE等研究的發(fā)現,當第一代EGFR-TKIs治療中出現T790M繼發(fā)突變時(shí),改用第三代EGFR-TKIs的序貫療法與直接使用第三代EGFR-TKIs相比,總生存期(OS)相似。然而,序貫治療組在顱內無(wú)進(jìn)展生存期(PFS)方面表現更佳。因此,對于攜帶經(jīng)典型突變的患者而言,第三代EGFR-TKIs已成為一線(xiàn)治療的優(yōu)選方案。不過(guò),目前尚缺乏第三代EGFR-TKIs之間的直接比較研究。
● 對于已使用 EGFR-TKIs 的 EGFR 經(jīng)典突變的 NSCLC 腦轉移患者出現繼發(fā) MET 擴增相關(guān)耐藥,可考慮聯(lián)合 Ib 類(lèi) MET-TKIs(2C)。
除了EGFR T790M突變,MET擴增或過(guò)表達同樣是EGFR陽(yáng)性患者在TKIs治療耐藥后常見(jiàn)的繼發(fā)性突變。對于這些對EGFR-TKIs治療產(chǎn)生耐藥性的NSCLC患者,聯(lián)合MET-TKIs治療已被初步證明能夠提高客觀(guān)緩解率(ORR)[17],盡管針對腦轉移患者的數據尚不充分。伯瑞替尼(Vebreltinib)的I/II期研究數據[18]表明,在接受過(guò)TKIs治療失敗并伴有MET擴增的腦轉移患者中,聯(lián)合使用第三代EGFR-TKIs可實(shí)現高達66.7%的ORR。此外,INSIGHT 2研究[19]的腦轉移亞組結果也表明,在第三代TKIs基礎上聯(lián)合使用特泊替尼(Tepotinib)后,繼發(fā)MET擴增的NSCLC患者的顱內ORR為29.2%,顱內疾病控制率(DCR)達到79.2%,其中25%的腦轉移患者實(shí)現了顱內完全緩解(CR)。
● 對靶向治療耐藥的 EGFR 突變 NSCLC 腦轉移患者,可考慮依沃西單抗聯(lián)合化療(2B)。
HARMONi-A研究[20]表明,對于EGFR-TKIs耐藥且基線(xiàn)存在腦轉移的患者,化療聯(lián)合依沃西單抗(Ivonescimab,一種針對VEGF和PD-1的雙特異性抗體)相較于安慰劑,顯著(zhù)延長(cháng)了PFS(5.75個(gè)月對比4.14個(gè)月,HR=0.40)。因此,對于靶向治療耐藥的EGFR突變NSCLC腦轉移患者,抗血管生成藥物與化療的聯(lián)合使用,也應被視為一種可行的治療方案。
● 對 EGFR ex20ins 突變的 NSCLC 腦轉移患者的二線(xiàn)靶向治療,推薦舒沃替尼治療(1B)。
WU-KONG6 II期臨床試驗[21]評價(jià)了舒沃替尼在中國EGFR ex20ins突變陽(yáng)性的局部晚期或轉移性NSCLC患者中的療效與安全性。受試者均經(jīng)過(guò)鉑類(lèi)化療,基線(xiàn)時(shí)31例(32%)合并腦轉移,舒沃替尼治療后的ORR為48%,提示舒沃替尼用于EGFR ex20ins陽(yáng)性NSCLC腦轉移的二線(xiàn)治療有一定的顱內活性,具有一線(xiàn)治療EGFR ex20ins突變的潛力。
● 對 EGFR PACC 突變的 NSCLC 腦轉移患者的一線(xiàn)靶向治療,可考慮高劑量伏美替尼治療(2C)。
在一項隨機、全球、多中心、I/II期臨床研究中,伏美替尼在一線(xiàn)治療EGFR PACC突變型NSCLC患者的全球Ib期FURTHER研究數據[22]顯示,在其240 mg qd劑量組中,ORR高達81.8%,在伴隨中樞神經(jīng)系統轉移的患者中,顱內ORR、DCR、CR率分別為46.2%、84.6%和38.5%,且耐受性良好。這一研究為EGFR PACC突變腦轉移一線(xiàn)靶向治療提供了新的治療選擇。
ALK
● 對于初治的 ALK 陽(yáng)性 NSCLC 腦轉移患者,優(yōu)選洛拉替尼(1B)、阿來(lái)替尼(1B)靶向治療,恩沙替尼、布格替尼、塞瑞替尼、依奉阿克、伊魯阿克等均可考慮(2B),克唑替尼僅應在其他第二、三代 ALK-TKIs 不可及的情況下選用(3B)。
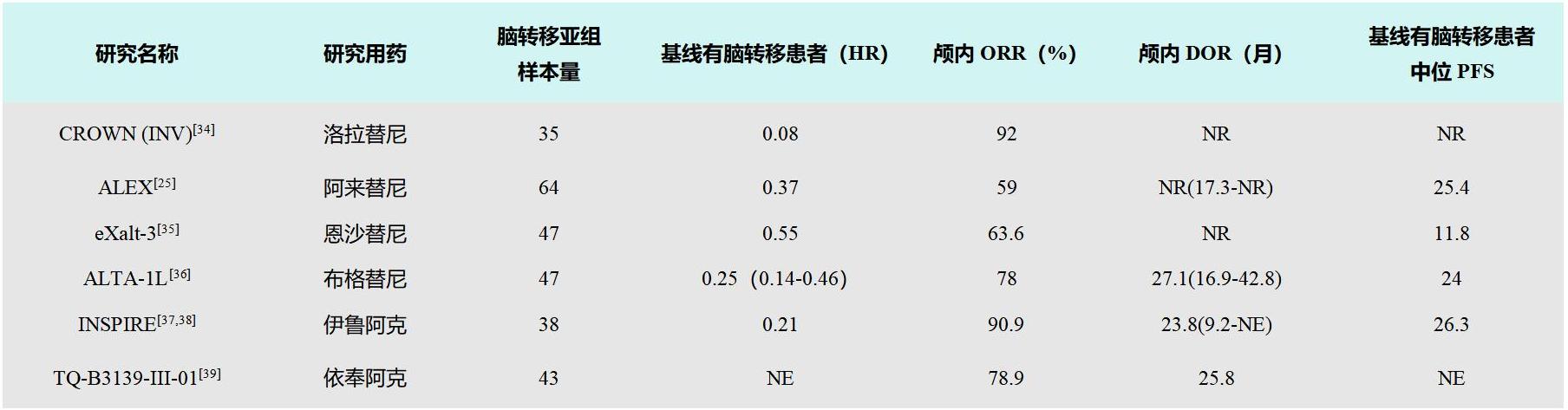
第二、三代藥物恩沙替尼(Ensartinib)[23]、布格替尼(Brigatinib)[24]、阿來(lái)替尼[25]、洛拉替尼[26]與克唑替尼有頭對頭的NSCLC一線(xiàn)治療用藥比較,PFS和/或OS結果均優(yōu)于克唑替尼,一定程度上解決了耐藥問(wèn)題。針對腦轉移,克唑替尼對中樞神經(jīng)系統的滲透率較差[27],第二、三代ALK-TK Is藥物的顱內活性增加,進(jìn)而改善預后。洛拉替尼的CROWN研究[28]和阿來(lái)替尼的ALEX研究[29]已經(jīng)隨訪(fǎng)超過(guò)5年,均有超過(guò)60%的受試者(包括腦轉移)實(shí)現長(cháng)生存。在CROWN研究[30]中,洛拉替尼經(jīng)過(guò)5年研究者隨訪(fǎng),較克唑替尼組至顱內進(jìn)展風(fēng)險降低97%,5年無(wú)顱內進(jìn)展率為83%,在基線(xiàn)可測量腦轉移患者中,隨訪(fǎng)5年ORR為92%,顱內CR為58%,整體人群PFS率為60%,提示洛拉替尼在PFS方面有較大優(yōu)勢。
● ALK 陽(yáng)性 NSCLC 腦轉移患者在應用克唑替尼耐藥后,如果無(wú)基因檢測提示繼發(fā)旁路激活的情況下可改換洛拉替尼(1B)或阿來(lái)替尼(2B)。
多項研究[31,32]提示可以后線(xiàn)使用洛拉替尼,顱內ORR仍可維持在80%以上;提示克唑替尼替尼耐藥的ALK陽(yáng)性腦轉移患者可考慮改換后代ALK抑制劑。至于第二、三代能否在耐藥后互換,洛拉替尼有數據[33]表明,對替代后線(xiàn)治療既往使用≥1種第二代ALK-TK Is±克唑替尼的患者,ORR為39.6%,中位PFS為6.6個(gè)月,基線(xiàn)可測量腦轉移患者顱內ORR為56.1%。
表2 ALK+ NSCLC一線(xiàn)ALK-TKIs治療腦轉移療效數據
Table2 Efficacy data of first-line ALK-TKIs treatment for brain metastases in ALK+ NSCLC
ROS1
● ROS1 陽(yáng)性 NSCLC 腦轉移患者初始用藥可考慮恩曲替尼(1B)、瑞普替尼(1B)、他雷替尼(1B)或安奈克替尼(1B);上述藥物如不可及,克唑替尼(2B)可作為替代用藥。
ROS1和ALK生理作用類(lèi)似,近一半的氨基酸序列是一致的,ATP結合位點(diǎn)的同源性更是超過(guò)了3/4[40],這種相似性使得部分ALK抑制劑(如克唑替尼)也兼具抑制ROS1的療效。克唑替尼是首個(gè)在NSCLC獲批的ROS1-TKIs,奠定了ROS1重排NSCLC患者的治療基石。相比克唑替尼,恩曲替尼(Entrectinib)、瑞普替尼(Repotrectinib)、安奈克替尼(Unecritinib)和他雷替尼(Taletrectinib)對ROS1的選擇性更優(yōu),表現出更優(yōu)的顱內ORR和PFS,并已在中國批準上市。恩曲替尼在一線(xiàn)治療ROS1融合陽(yáng)性NSCLC腦轉移患者中,中位PFS為14.9個(gè)月,中位OS長(cháng)達28.3個(gè)月,且安全性良好[41];STARTRK系列和ALKA研究匯總分析也證實(shí)恩曲替尼具有較高的顱內ORR[42]。TRIDENT-1試驗[43]中,瑞普替尼在具有可測量CNS轉移的初治患者中顯示出88%的顱內ORR,對于接受過(guò)其他ROS1-TKIs治療的患者,顱內反應率依然有42%。II期TQ-B3101研究[44]顯示安奈克替尼整體人群ORR達81.08%;對于伴腦轉移患者的ORR為72.73%,中位OS為28.22個(gè)月;在常見(jiàn)ROS1融合(CD74)中及既往化療人群中療效較整體人群更佳。

所有患者、有基線(xiàn)研究者評估的中樞神經(jīng)系統轉移的患者以及無(wú)基線(xiàn)研究者評估的中樞神經(jīng)系統轉移的患者的中樞神經(jīng)系統進(jìn)展時(shí)間
Time to CNS progression (deaths censored) in all patients, patients with baseline investigator-assessed CNS metastases, and patients without baseline investigator-assessed CNS metastases.[41]
NTRK
● 對 NTRK 陽(yáng)性初治 NSCLC 腦轉移患者,可考慮應用恩曲替尼(1B)或拉羅替尼(1B)靶向治療。
在NSCLC腦轉移有循證支持的TRK抑制劑目前有拉羅替尼(Larotrectinib)和恩曲替尼。拉羅替尼是兼具高選擇性和中樞活性的TRK抑制劑。包含2項拉羅替尼研究的匯總分析[45]發(fā)現,在納入的32例NTRK陽(yáng)性的NSCLC中有12例合并腦轉移,經(jīng)拉羅替尼治療后ORR為67%(8/12)。由于NTR K和ROS1也有一定的同源性,因此恩曲替尼也能用于NTRK陽(yáng)性NSCLC患者。恩曲替尼顱內ORR在60%以上(9/14),顱內PFS中位數為32.7個(gè)月[46];但總的來(lái)說(shuō),NTRK靶向藥物涉及的多為泛腫瘤的籃子研究,受試者納入沒(méi)有嚴格限制,協(xié)作組認為目前針對NTRK融合NSCLC腦轉移靶向治療循證雖然有限但獲益明確,因此及早啟用NTRK靶向治療應是合理的。

恩曲替尼治療時(shí)間和總體反應
Time on entrectinib treatment and best overall response[46]
RET
● RET 融合陽(yáng)性的初治 NSCLC 腦轉移患者,一線(xiàn)全身治療推薦高選擇性 RET 抑制劑如塞普替尼(1B)和普拉替尼(2B)。
RET基因融合往往發(fā)生于臨床分期較晚的患者,因此RET融合雖在NSCLC的發(fā)生率不高,但32.2%的RET融合NSCLC患者在初診時(shí)伴有腦轉移[47],這一比例在我國更高(40.3%)[48]。塞普替尼(Selpercatinib)和普拉替尼(Pralsetinib)是目前臨床應用最多的選擇性RET抑制劑。LIBR ETTO-431研究[49]比較了一線(xiàn)塞普替尼與標準治療[含鉑化療±帕博利珠單抗(Pembrolizumab)]對RET融合陽(yáng)性NSCLC患者的療效和安全性;基線(xiàn)腦轉移亞組(n=42)中,塞普替尼顱內ORR為82%,其中6例達到CR,12個(gè)月的顱內持續應答率為72%;并在東亞人群中顯示出較高的顱內ORR(81%)[50]。普拉替尼也顯示出同等水平的顱內活性,ARROW研究[51]中國NSCLC腦轉移亞組顯示,普拉替尼一線(xiàn)治療ORR為85.7%,DCR為85.7%,但樣本量較少(n=7)。


通過(guò)盲法獨立中心審查評估無(wú)進(jìn)展生存期
Progression-Free Survival Assessed by Blinded Independent Central Review[49]
KRAS G12C
● 對KRAS G12C突變的 NSCLC 腦轉移患者,推薦氟澤雷塞(1B)、格索雷塞(1B)二線(xiàn)治療,鼓勵患者進(jìn)行一線(xiàn)聯(lián)合的臨床研究試驗。
最早在國外上市的兩款KR ASG12C靶向藥物——索托拉西布(Sotorasib)和阿達拉西布(Adagrasib),雖然有腦轉移的證據,但目前均未在中國上市。目前,我國已有兩款新上市的KR AS G12C抑制劑氟澤雷塞(Fulzerasib)和格索雷塞(Garsorasib),獲批適應證均為KRAS G12C突變晚期NSCLC的二線(xiàn)治療。
研究[52]提出EGFR與KR AS G12C抑制劑聯(lián)合治療的策略,因為KRAS G12C抑制劑阻斷RAS通路后,可能導致EGFR再激活。KROCUS研究[53]初步結果顯示,氟澤雷塞聯(lián)合西妥昔單抗治療基線(xiàn)時(shí)有腦轉移且KRAS G12C突變陽(yáng)性的NSCLC患者,總體ORR達到了80%;其中,71.4%的腦轉移患者實(shí)現了病理緩解。盡管樣本量有限,鑒于目前KRAS G12C突變靶向治療顱內ORR和PFS欠佳,這一聯(lián)合療法無(wú)疑帶來(lái)了新選擇。


KRAS G12C和EGFR抑制劑對KRAS G12C抑制作用的數學(xué)模型發(fā)現RAS網(wǎng)絡(luò )蛋白的生物物理特性以及RAS和EGFR抑制劑足以解釋野生型和突變型RAS的共靶向作用
Mathematical modeling of KRAS G12C inhibition by the KRAS G12C and EGFR inhibitors finds the biophysical properties of the RAS network proteins and the RAS and EGFR inhibitors are sufficient to explain the co-targeting of wild-type and mutant RAS.[52]
MET ex14
● 對 METex14 跳躍突變的 NSCLC 腦轉移患者一線(xiàn)或二線(xiàn)靶向治療,優(yōu)先選擇有顱內活性證據的 Ib 類(lèi) MET 抑制劑,如伯瑞替尼、特泊替尼、卡馬替尼、谷美替尼和賽沃替尼(2B)。
KUNPENG研究[54]證實(shí),對晚期METex14跳躍突變的中國NSCLC患者,伯瑞替尼治療晚期METex14跳躍突變的中國NSCLC患者的中位PFS為14.1個(gè)月,OS為20.7個(gè)月,其中腦轉移亞組(n=5)中位PFS較短為6.4個(gè)月,OS為17.9個(gè)月。值得一提的是,伯瑞替尼是目前唯一具有肺癌及腦膠質(zhì)瘤適應證的MET抑制劑。VISION研究(單臂II期)腦轉移亞組結果[55]顯示,通過(guò)RANO -BM標準進(jìn)行評估,特泊替尼在初治和經(jīng)治METex14跳躍突變患者中的顱內ORR為66.7%,顱內DCR為88.4%,顱內中位PFS為20.9個(gè)月,顯示出持久的抗腫瘤活性。盡管臨床上可用的針對MET突變的藥物數量不斷涌現,但腦轉移人群的證據不多,集中在共識或指南優(yōu)選的Ib類(lèi)MET抑制劑循證。大多數Ib類(lèi)抑制劑均能夠有效通過(guò)BBB[56]。

由盲法獨立審查委員會(huì )評估的伯瑞替尼的抗腫瘤活性。(A)患者的治療暴露和反應持續時(shí)間。
Antitumor activity of vebreltinib as assessed by blinded independent review committee. (A) Treatment exposure and response duration of patients.[54]
HER2
● 鼓勵HER2突變陽(yáng)性 NSCLC 腦轉移患者參加一線(xiàn) HER2-TKIs 臨床研究,二線(xiàn)及后線(xiàn)靶向治療推薦德曲妥珠單抗(1B)或吡咯替尼(2C)。
NSCLC中,HER2基因異常主要表現為基因擴增/過(guò)表達和突變(主要為ex20ins突變)的形式,而后者更為常見(jiàn)[57]。HER2陽(yáng)性NSCLC腦轉移靶向治療的重點(diǎn)是針對HER2突變(特別是針對20ins或YVMA插入)的抗體偶聯(lián)藥物(antibody-drug conjugate, ADC)或TKIs。HER2 - ADC方面,已經(jīng)上市的有恩美曲妥珠單抗(Ado-trastuzumab emtansine, T-DM1)和德曲妥珠單抗(Trastuzumab deruxtecan, T-DXd)。恩美曲妥珠單抗雖然在NSCLC H ER 2靶向治療的臨床研究開(kāi)展較早,但很少涉及腦轉移人群[58]。德曲妥珠單抗則后來(lái)者居上,在DESTINY-Lung02研究的腦轉移亞組(n=20)中,顯示出良好的療效,ORR為64.3%(9/14),其中包括7例CR,顱內反應持續時(shí)間為55.7個(gè)月。此外,DESTIN Y-Lung01研究[59]中也納入了33例伴有腦轉移的患者,其ORR為54.5%,中位PFS為7.1個(gè)月,中位OS為13.8個(gè)月。近期,中國國家藥品監督管理局批準了德曲妥珠單抗用于HER2突變晚期不可切除或轉移性NSCLC二線(xiàn)及以上治療的適應證。
吡咯替尼(Pyrotinib)是我國應用廣泛的一種HER2-TKIs。在一項I I期多中心研究[60]中,納入化療經(jīng)治后的HER 2陽(yáng)性NSCLC患者,二線(xiàn)應用吡咯替尼后整體ORR為30%,腦轉移亞組略低(25%),整體的PFS和OS分別為6.9和14.4個(gè)月。也有研究[61]指出將吡咯替尼與阿帕替尼(Apatinib,小分子V EGFR-2抑制劑)聯(lián)合使用,提升了基線(xiàn)伴腦轉移HER 2+患者(n=13)的OR R至53.8%。

抗腫瘤活性。(A)顯示91名患者中的85名患者的可測量腫瘤的直徑總和相對于基線(xiàn)的百分比變化,患者的目標病變的基線(xiàn)和基線(xiàn)后評估數據均通過(guò)獨立中心審查。
Antitumor Activity.(A) shows the best percentage change from baseline in the sum of the largest diameters of measurable tumors in 85 of 91 patients for whom data from both baseline and postbaseline assessments of target lesions by independent central review were available.[59]
BRAF V600
● 對BRAF V600突變的 NSCLC 腦轉移患者,可考慮達拉非尼聯(lián)合曲美替尼治療(2C)或康奈非尼聯(lián)合比美替尼治療(3C)。
由于單一使用BRAF抑制劑達拉非尼(Dabrafenib)很容易出現耐藥,通常聯(lián)用MEK抑制劑曲美替尼(Trametinib),目前這一組合已成為NSCLC BRAFV600突變的標準靶向治療。在一項達拉非尼和曲美替尼治療BRAF V600E突變NSCLC研究[62]的腦轉移亞組中(n=34),聯(lián)合治療后觀(guān)察到25例(80.6%)達到客觀(guān)緩解,中位PFS為7.5個(gè)月,中位OS達24.1個(gè)月。在達拉非尼和曲美替尼II期關(guān)鍵性臨床研究[63]中,雖排除活動(dòng)性腦轉移,但仍納入了3例基線(xiàn)腦轉移病灶為非靶病灶的患者,無(wú)論一線(xiàn)還是后線(xiàn)療效均達到PR,治療后未有新發(fā)腦轉移進(jìn)展。此外,還有個(gè)例報道[64, 65]探索了達拉非尼、曲美替尼用于一線(xiàn)治療BR AF V600突變腦轉移患者腦部病灶均達到完全緩解。

NGS在接受達拉非尼和曲美替尼治療的轉移性非小細胞肺癌患者的檔案活檢中檢測到的基因組改變及其與臨床結果的相關(guān)性
Genomic Alterations Detected by NGS in Archival Biopsies From Patients With Metastatic NSCLC Treated With Dabrafenib and Trametinib and Association With Clinical Outcomes[62]
總之,中樞神經(jīng)系統轉移一直被視為晚期實(shí)體瘤的一種毀滅性并發(fā)癥。在過(guò)去十年中,盡管眾多新型療法迅速發(fā)展,使顱外腫瘤控制得到改善,但包括腦膜轉移在內的中樞神經(jīng)系統轉移正成為日益突出的未滿(mǎn)足需求,可能限制患者的長(cháng)期生存。由于腫瘤細胞位于由血腦屏障保護的生理獨特區域,中樞神經(jīng)系統轉移被認為是一個(gè)獨特的挑戰,因此需要不同的治療策略。對于由致癌基因驅動(dòng)的非小細胞肺癌患者,一系列具有出色腦滲透性的新型酪氨酸激酶抑制劑(TKIs)已經(jīng)在攜帶某些驅動(dòng)致癌基因的患者亞群中取得了臨床成功。與此同時(shí),放化療技術(shù)和外科技術(shù)的進(jìn)步不斷改善治療效果,但同時(shí)也使中樞神經(jīng)系統轉移的管理變得高度復雜且多學(xué)科化,需要密切協(xié)作。新型診斷和鞘內治療技術(shù)也在不斷拓展治療中樞神經(jīng)系統轉移和腦膜轉移患者的潛力。隨著(zhù)發(fā)展隨著(zhù)綜合療效評估標準的改進(jìn)以及指導針對中樞神經(jīng)系統轉移瘤患者未滿(mǎn)足需求的藥物開(kāi)發(fā)的監管建議的出臺,預計未來(lái)幾年這一領(lǐng)域的臨床研究將大幅增長(cháng),最終改善患者的臨床結局。
參考文獻
[1] Nat Rev Clin Oncol. 2023;20(10):716-732.
[2] Zhongguo Fei Ai Za Zhi. Published online January 7, 2025.
[3] J Clin Oncol, 2024, 42(7): 808-820.
[4] J Thorac Oncol, 2022, 17(11): 1297-1305.
[5] Lancet Respir Med, 2023, 11(10): 905-915.
[6] J Clin Oncol , 2022,40(16_suppl): 9096.
[7] Med, 2024: S2666-6340(24)00344-1.
[8] Lancet Respir Med, 2017, 5(9): 707-716.
[9] N Engl J Med, 2024, 391(16):1486-1498.
[10] Clin Cancer Res, 2021, 27(1): 189-201.
[11] Lancet Respir Med, 2017, 5(11): 891-902 .
[12] Med,2024:S2666-6340(24)00344-1.
[13] Lancet Respir Med,2017,5(11):891-902 .
[14] J Clin Oncol, 2018: JCO2018783118.
[15] J Clin Oncol , 2022,40(16_suppl): 9096. d
[16] J Clin Oncol, 2024, 42(12): 1350-1356.
[17] Cancer Discov, 2023, 13(1): 98-113.
[18] J Thorac Oncol, 2024, 19(10 Suppl): S105-S106.
[19] Lancet Oncol, 2024, 25(8): 989-1002.
[20] JAMA, 2024, 332(7): 561-570.
[21] Lancet Respir Med, 2024, 12(3): 217-224.
[22] J Thorac Oncol, 2024, 19(10 Suppl): S5-S6.
[23] JAMA Oncol, 2021, 7(11): 1617-1625.
[24] J Thorac Oncol, 2021, 16(12): 2091-2108.
[25] N Engl J Med, 2017, 377(9): 829-838.
[26] Lancet Respir Med, 2023, 11(4): 354-366.
[27] J Clin Oncol, 2011,29(15): e443-e445.
[28] Cancers (Basel), 2024, 16(13): 2457.
[29] Ann Oncol, 2020, 31(8): 1056-1064.
[30] J Clin Oncol, 202 4, 42(29): 3400-3409.
[31] J Clin Oncol, 2018, 36(15_suppl): 9032.
[32] J Thorac Oncol, 2022, 17(6): 816-826.
[33] Ann Oncol, 2021, 32(5): 620-630.
[34] J Clin Oncol, 2024,42(29): 3400-3409.
[35] JA M A Oncol, 2021, 7(11): 1617-1625.
[36] J Clin Oncol,2020, 38(31): 3592-3603.
[37] J Thorac Oncol, 2024, 19(6): 855-857.
[38] Ann Oncol, 2024, 35(suppl_2): 1278P.
[39] Signal Transduct Target Ther,2023, 8(1): 301.
[40] N Engl J Med, 2014, 371(21): 1963-1971.
[41] JTO Clin Res Rep, 2022, 3(6): 100332.
[42] Lancet Oncol, 2020, 21(2): 261-270.
[43] J Clin Oncol, 2023, 41(16_suppl): 9017.
[44] Signal Transduct Target Ther, 2023, 8(1): 249.
[45] J Clin Oncol, 2023, 41(16_suppl): 9056.
[46] Lung Cancer, 2024, 188: 107442.
[47] J Thorac Oncol, 2023, 18(12): 1703-1713.
[48] Transl Lung Cancer Res, 2022, 11(4): 617-631.
[49] N Engl J Med, 2023, 389(20): 1839-1850.
[50] J Clin Oncol, 2024, 42(23_ suppl): 214.
[51] Cancer, 2023, 129(20): 3239-3251.
[52] NPJ Precis Oncol, 2022, 6(1): 86.
[53] J Clin Oncol , 2024 , 42(17_suppl): LBA8511.
[54] J Clin Oncol, 2024, 42(31): 3680-3691.
[55] J Thorac Oncol, 2022, 17(9): S9-S10.
[56] Cell, 2018, 175(6): 1665-1678.e18.
[57] Cancers (Basel), 2022, 14(17): 4155.
[58] J Clin Oncol, 2018, 36(24): 2532-2537.
[59] N Engl J Med, 2022, 386(3): 241-251.
[60] J Clin Oncol, 2020, 38(24): 2753-2761.
[61] BMC Med, 2022, 20(1): 277.
[62] J Thorac Oncol, 2022, 17(1): 103-115.
[63] Lancet Oncol, 2016, 17(7): 984-993.
[64] Clin Lung Cancer, 2020, 21(6): e544-e546.
[65] J Thorac Oncol, 2019, 14(5): e97-e99.